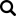Phivax BD-1 liofilizat i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań dla kur
Każda dawka zawiera:
Substancja czynna:
Żywy, atenuowany, pośredni szczep M.B. wirusa zakaźnego zapalenia torby Fabrycjusza ptaków 101,5
do 102,5 EID50 *
*EID 50 dawka zakaźna dla 50% jaj
Substancje pomocnicze:
Liofilizat: brązowawy
Rozpuszczalnik: bezbarwny
3.1. Docelowe gatunki zwierząt
Kura (brojler, nioska, ptaki stad zarodowych lub hodowlanych)
3.2. Wskazania lecznicze dla każdego z docelowych gatunków zwierząt
Szczepionka jest wskazana do czynnego uodparniania kurcząt, u których poziom przeciwciał matczynych jest wyższy niż 2500 jednostek ELISA, w celu zmniejszenia śmiertelności i nasilenia zmian chorobowych związanych z zakażeniem wirusem IBD.
Czas powstania odporności: 21. dzień życia, w zależności od początkowego poziomu przeciwciał matczynych (odporność jest uzależniona od naturalnego spadku poziomu przeciwciał matczynych i związanego z nim stopnia uwalniania wirusa szczepionkowego).
Czas trwania odporności: 42 dni.
3.3. Przeciwwskazania
Brak
3.4. Specjalne ostrzeżenia
Należy szczepić tylko zdrowe zwierzęta.
Zarodki kurze w 18. dniu inkubacji:
Iniekcja metodą in ovo musi być wykonana sprzętem przeznaczonym do wykonywania tego typu szczepienia. Urządzenia wykorzystywane do rozpuszczania szczepionki, jak i do szczepienia powinny być sterylne i wolne od jakichkolwiek pozostałości chemicznych środków dezynfekcyjnych.
Sprzęt powinien zapewniać bezpieczne i skuteczne podanie jednej dawki szczepionki (0,05-0,1 ml) bezpośrednio do owodni lub zarodka.
Przed każdą iniekcją in ovo technikę szczepienia należy sprawdzić przez zastosowanie zabarwionego roztworu. Należy ściśle przestrzegać zaleceń producenta sprzętu wykorzystywanego do szczepienia. Do czyszczenia sprzętu należy stosować wyłącznie środki zatwierdzone przez wytwórcę. Zaleca się stosowanie igieł o następujących parametrach: 0,4 – 0,8 mm średnicy, 25-28 mm długości oraz 3,5 – 5 bar (50 psi – 72 psi).
Pisklęta jednodniowe:
Do podskórnego podania szczepionki można wykorzystywać strzykawki automatyczne. Urządzenia wykorzystywane do rozpuszczania szczepionki, jak i do szczepienia powinny być sterylne i wolne od jakichkolwiek pozostałości chemicznych środków dezynfekcyjnych.
Sprzęt powinien zapewniać bezpieczne i skuteczne podanie jednej dawki szczepionki (0,1 – 0,2 ml). Należy ściśle przestrzegać zaleceń producenta sprzętu wykorzystywanego do szczepienia.
Szczepionkę należy podawać pod skórę na karku jednodniowych kurcząt brojlerów.
Pobieranie próbek do badania poziomu przeciwciał matczynych, jak również program szczepień należy zawsze skonsultować z lekarzem weterynarii.
3.5. Specjalne środki ostrożności dotyczące stosowania
Specjalne środki ostrożności dotyczące bezpiecznego stosowania u docelowych gatunków zwierząt:
U ptaków nieposiadających przeciwciał matczynych podanie szczepionki może spowodować znaczną immunosupresję i uszkodzenie torby Fabrycjusza. Dlatego nie zaleca się szczepienia 18-dniowych zalężonych jaj oraz piskląt, pochodzących ze stad z mianami przeciwciał matczynych (u 1-dniowych piskląt) niższymi niż 2500 (test IDEXX-ELISA).
Zaleca się przeprowadzenie wstępnego badania w celu ustalenia poziomów przeciwciał matczynych u piskląt: należy pobrać próbki od 20 jednodniowych piskląt pochodzących z tego samego stada hodowlanego w celu określenia ich statusu serologicznego w kierunku wirusa IBD. Wyniki badań wskażą czy poziom przeciwciał matczynych może osiągnąć u piskląt pochodzących z badanego stada oczekiwaną wartość przynajmniej 2500 jednostek ELISA w kolejnych 4 tygodniach. W zależności od uzyskanych wyników i oczekiwań, badanie to może być powtarzane w różnych momentach okresu nieśności.
Z uwagi na fakt, że szczepionkę podaje się podskórnie u jednodniowych piskląt lub metodą in ovo w przypadku 18-dniowych zalężonych jaj, należy zachować szczególną ostrożność w celu uniknięcia zanieczyszczenia szczepionki lub wykorzystywanego sprzętu w trakcie szczepienia. Szczep szczepionkowy może przenosić się na ptaki nieszczepione przez kontakt. Aby zapobiec rozprzestrzenianiu się wirusa, po szczepieniu należy odkazić zarówno sprzęt stosowany do szczepienia, jak i pomieszczenia wylęgarni. Pisklęta pochodzące z zaszczepionych jaj nie powinny być łączone z pisklętami pochodzącymi z jaj niezaszczepionych. Analogicznie, nie należy łączyć zaszczepionych jednodniowych piskląt z pisklętami nieszczepionymi.
Specjalne środki ostrożności dla osób podających weterynaryjny produkt leczniczy zwierzętom:
Po przypadkowej samoiniekcji, należy niezwłocznie zwrócić się o pomoc lekarską oraz przedstawić lekarzowi ulotkę informacyjną lub opakowanie (nawet jeśli wstrzyknięta została niewielka ilość produktu).
Po zakończeniu pracy z weterynaryjnym produktem leczniczym należy umyć i zdezynfekować ręce zatwierdzonym środkiem do dezynfekcji.
Specjalne środki ostrożności dotyczące ochrony środowiska:
Nie dotyczy.
3.6. Działania niepożądane
Kura:
![]()
* maksymalne wartości osiągane są w 28 dniu po szczepieniu metodą in ovo i w 21 dniu po podaniu podskórnym. Po tym okresie dochodzi do ponownego namnożenia limfocytów i regeneracji torby Fabrycjusza. Przejściowy spadek ilości limfocytów nie powodował działania immunosupresyjnego.
Zgłaszanie zdarzenie niepożądanych jest istotne, ponieważ umożliwia ciągłe monitorowanie bezpieczeństwa stosowania weterynaryjnego produktu leczniczego. Zgłoszenia najlepiej przesłać za pośrednictwem lekarza weterynarii do właściwych organów krajowych lub do podmiotu odpowiedzialnego za pośrednictwem krajowego systemu zgłaszania. Właściwe dane kontaktowe znajdują się w ulotce informacyjnej.
3.7. Stosowanie w ciąży, podczas laktacji lub w okresie nieśności
Ptaki nieśne:
Nie stosować u ptaków w okresie nieśności i na 4 tygodnie przed rozpoczęciem okresu nieśności.
3.8. Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Dane dotyczące bezpieczeństwa i skuteczności wskazują, że szczepionka może być podawana w tym samym dniu, co żywe szczepionki przeciw chorobie Newcastle, ale nie zmieszana. Brak informacji dotyczących bezpieczeństwa i skuteczności szczepionki stosowanej jednocześnie z innym weterynaryjnym produktem leczniczym oprócz produktów wymienionych powyżej. W związku z tym decyzja o zastosowaniu szczepionki przed lub po podaniu innego weterynaryjnego produktu leczniczego powinna być podejmowana indywidualnie.
3.9. Droga podania i dawkowanie
Jedna dawka podana do jaja (0,05-0,1 ml) w przypadku 18-dniowych zalężonych jaj lub w formie iniekcji podskórnej (0,1-0,2 ml) u jednodniowych piskląt.
Podanie do jaja:
Rozpuścić szczepionkę w rozpuszczalniku (roztworze mleczanu sodu).
Produkt po rekonstytucji jest beżową, mętną zawiesiną. Szczepionka nie powinna być użyta, jeśli liofilizat („ciastko”) na dnie fiolki nie rozpuścił się całkowicie lub w ogóle nie jest rozpuszczony, a także jeśli „ciastko” ma niewłaściwy wygląd, np. zmieniony kolor lub wydaje się spuchnięte.
Szczepienie zalężonych jaj należy wykonać natychmiast po rekonstytucji szczepionki.
Wstrzykiwana objętość (dawka) wynosi przy podaniu in ovo 0,05 – 0,1 ml.
Szczepionkę podaje się za pomocą sprzętu przeznaczonego do inokulacji in ovo. Do szczepień tą metodą można wykorzystywać automatyczne urządzenia do szczepień in ovo. Sprzęt przeznaczony do szczepień in ovo należy stosować zgodnie z zaleceniami producenta. Przed przystąpieniem do szczepienia należy potwierdzić prawidłowość dawkowania.
Podanie podskórne:
Rozpuścić szczepionkę w rozpuszczalniku (roztworze mleczanu sodu).
Produkt po rekonstytucji jest beżową, mętną zawiesiną. Szczepionka nie powinna być użyta, jeśli liofilizat („ciastko”) na dnie fiolki nie rozpuścił się całkowicie lub w ogóle nie jest rozpuszczony, a także jeśli „ciastko” ma niewłaściwy wygląd, np. zmieniony kolor lub wydaje się spuchnięte.
Szczepienie jednodniowych piskląt należy wykonać natychmiast po rekonstytucji szczepionki.
Dawkę 0,1 – 0,2 ml rozpuszczonej szczepionki na pisklę, należy podać podskórnie w tylną część karku. Do szczepienia można wykorzystywać zarówno strzykawki tradycyjne jak i automatyczne, jak również maszyny do szczepienia.
Do rozpuszczania i podawania szczepionki należy używać wyłącznie sterylnych narzędzi i sprzętu.
Rozpuszczanie szczepionki
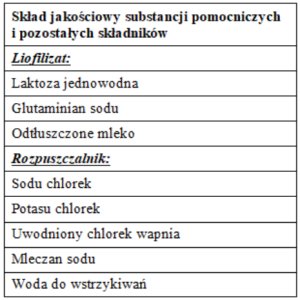
Do podania podskórnego (s.c.) w pierwszym dniu życia, w dawce 0,1 – 0,2 ml
1. Obliczyć i przygotować wymaganą objętość rozpuszczonej szczepionki w następujący sposób:
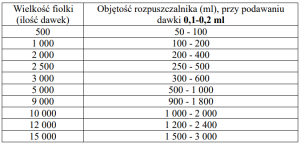
2. Pobrać 2 ml rozpuszczalnika i przenieść do szklanej fiolki zawierającej liofilizat.
3. Dokładnie rozpuścić szczepionkę – delikatnie wstrząsając, a następnie przenieść do opakowania rozpuszczalnika.
4. Przepłukać fiolkę dodając kolejne 2 ml rozpuszczalnika i ponownie przenieść otrzymany roztwór do opakowania rozpuszczalnika.
Do szczepienia in-ovo w 18-tym dniu inkubacji, w dawce 0,05 – 0,1 ml
1. Obliczyć i przygotować wymaganą objętość rozpuszczonej szczepionki w następujący sposób:
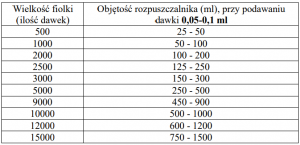
2. Pobrać 2 ml rozpuszczalnika i przenieść do szklanej fiolki zawierającej liofilizat.
3. Dokładnie rozpuścić szczepionkę delikatnie wstrząsając, a następnie przenieść do opakowania rozpuszczalnika.
4. Przepłukać fiolkę dodając kolejne 2 ml rozpuszczalnika i ponownie przenieść otrzymany roztwór do opakowania rozpuszczalnika.
Podanie szczepionki:
Należy przestrzegać instrukcji obsługi automatycznych strzykawek lub używanego sprzętu.
Należy zachować szczególną ostrożność w celu uniknięcia zanieczyszczenia szczepionki lub sprzętu w czasie szczepienia.
Należy zawsze używać sterylnych igieł i wężyków.
3.10. Objawy przedawkowania (oraz sposób postępowania przy udzielaniu natychmiastowej pomocy i odtrutki, w stosownych przypadkach)
W badaniach dotyczących przedawkowania potwierdzono, że przy 10-krotnym przedawkowaniu spadek ilości limfocytów w torbie Fabrycjusza jest bardzo częsty, osiągając maksymalne wartości w 35 dniu po szczepieniu metodą in ovo i w 21 dniu po podaniu podskórnym. Przejściowy spadek ilości limfocytów nie powodował działania immunosupresyjnego.
3.11. Szczególne ograniczenia dotyczące stosowania i specjalne warunki stosowania, w tym ograniczenia dotyczące stosowania przeciwdrobnoustrojowych i przeciwpasożytniczych weterynaryjnych produktów leczniczych w celu ograniczenia ryzyka rozwoju oporności
Nie dotyczy.
3.12. Okresy karencji
Zero dni.
4.1. Kod ATCvet:
QI01AD09
Szczepionka stymuluje wczesną, aktywną odporność przeciw wirulentnym szczepom wirusa zakaźnego zapalenia torby Fabrycjusza (choroby Gumboro). Szczep M.B. zawarty w szczepionce jest klasyfikowany jako szczep pośredni wirusa IBD. Szczepionka nie wykazuje jednak działania immunosupresyjnego.
5.1 Główne niezgodności farmaceutyczne
Nie mieszać z innym weterynaryjnym produktem leczniczym, z wyjątkiem rozpuszczalnika zalecanego do stosowania z weterynaryjnym produktem leczniczym.
5.2 Okres ważności
Okres ważności weterynaryjnego produktu leczniczego zapakowanego do sprzedaży: 2 lata.
Okres ważności rozpuszczalnika zapakowanego do sprzedaży: 3 lata.
Okres ważności po rekonstytucji zgodnie z instrukcją: 4 godziny.
5.3 Specjalne środki ostrożności przy przechowywania
Liofilizat:
Przechowywać w lodówce (2°C–8°C).
Chronić przed światłem.
Rozpuszczalnik:
Przechowywać w temperaturze poniżej 25°C.
5.4 Rodzaj i skład opakowania bezpośredniego
Liofilizat:
Szklana fiolka o klasie hydrolitycznej I, zamknięta korkiem z gumy bromobutylowej i uszczelniona aluminiowym kapslem.
Wielkości opakowań: fiolki zawierające 500, 1000, 2000, 2500, 3000, 5000, 9000, 10000, 12000 lub 15000 dawek, pakowane w pudełka tekturowe po 10 sztuk.
Rozpuszczalnik:
Butelka z LDPE zawierająca 500 ml lub 1000 ml rozpuszczalnika.
Niektóre wielkości opakowań mogą nie być dostępne w obrocie.
5.5. Specjalne środki ostrożności dotyczące usuwania niezużytych weterynaryjnych produktów leczniczych lub pochodzących z nich odpadów
Leków nie należy usuwać do kanalizacji ani wyrzucać do śmieci.
Należy skorzystać z krajowego systemu odbioru odpadów w celu usunięcia niewykorzystanego weterynaryjnego produktu leczniczego lub materiałów odpadowych pochodzących z jego zastosowania w sposób zgodny z obowiązującymi przepisami oraz krajowymi systemami odbioru odpadów dotyczącymi danego weterynaryjnego produktu leczniczego.
Phibro Animal Health (Poland) Sp. z o.o.
ul. Towarowa 28
00-839 Warszawa
Polska
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 16.03.2020
ZAKAZ WYTWARZANIA, IMPORTU, POSIADANIA, SPRZEDAŻY, DOSTAWY I/LUB
STOSOWANIA
02/2025