TAbic IB VAR tabletka musująca do sporządzania zawiesiny dla kur
1 dawka szczepionki zawiera:
Substancje czynne:
Wirus zakaźnego zapalenia oskrzeli ptaków, szczep 233A war-1, żywy nie mniej niż 103,2 EID50 i nie więcej niż 105,1 EID50*
*EID50 = dawka zakaźna dla 50% zarodków. (Statystycznie określona ilość wirusa, która może
zainfekować 50% zapłodnionych jaj, do których został zaszczepiony).
Substancje pomocnicze:

Okrągła tabletka musująca barwy białawej.
3.1 Docelowe gatunki zwierząt
Kury (brojlery, nioski i stada reprodukcyjne).
3.2 Wskazania lecznicze dla każdego z docelowych gatunków zwierząt
Czynne uodparnianie kurcząt brojlerów, niosek i stad reprodukcyjnych w celu zredukowania śmiertelności, objawów klinicznych oraz zmian towarzyszących zakaźnemu zapaleniu oskrzeli
ptaków.
Szczepienia można przeprowadzać w każdym wieku, począwszy od pierwszego dnia życia. Jednokrotne szczepienie powoduje szybkie narastanie odporności przeciw wirusowi zakaźnego
zapalenia oskrzeli ptaków. Nioski i stada reprodukcyjne należy doszczepiać również w późniejszym wieku, zgodnie z ustalonym programem szczepień.
Czas powstania odporności: 21 dni po szczepieniu.
Czas trwania odporności: 42 dni po szczepieniu. Dwukrotne szczepienie ptaków (w 1-szym i 14-stym
dniu życia) w pełni zabezpiecza stada brojlerów do czasu uboju w 7-8 tygodniu życia.
3.3 Przeciwwskazania
Nie szczepić ptaków wykazujących kliniczne objawy choroby lub narażonych na działanie czynników
stresogennych.
3.4 Specjalne ostrzeżenia
Należy szczepić tylko zdrowe zwierzęta
3.5 Specjalne środki ostrożności dotyczące stosowania
Specjalne środki ostrożności dotyczące bezpiecznego stosowania u docelowych gatunków zwierząt:
Immunokompetencja zwierzęcia może być obniżona przez różne czynniki, w tym choroby immunosupresyjne, stan odżywienia i stres. Szczep szczepionkowy może przenosić się na podatne gatunki. Należy zachować specjalne środki ostrożności w celu uniknięcia rozprzestrzeniania się szczepu szczepionkowego na podatne gatunki.
Specjalne środki ostrożności dla osób podających weterynaryjny produkt leczniczy zwierzętom:
Podczas stosowania weterynaryjnego produktu leczniczego należy używać środków ochrony osobistej, na które składają się rękawice, okulary i maska ochronna. Po przypadkowym połknięciu lub rozlaniu na skórę, należy niezwłocznie zwrócić się o pomoc lekarską oraz przedstawić lekarzowi ulotkę informacyjną lub opakowanie.
Specjalne środki ostrożności dotyczące ochrony środowiska:
Nie dotyczy
3.6 Zdarzenia niepożądane
Brak.
Zgłaszanie zdarzeń niepożądanych jest istotne, ponieważ umożliwia ciągłe monitorowanie bezpieczeństwa stosowania weterynaryjnego produktu leczniczego. Zgłoszenia najlepiej przesłać za
pośrednictwem lekarza weterynarii do podmiotu odpowiedzialnego lub jego lokalnego przedstawiciela lub do właściwych organów krajowych za pośrednictwem krajowego systemu zgłaszania. Właściwe dane kontaktowe znajdują się w ulotce informacyjnej.
3.7. Stosowanie w ciąży, podczas laktacji lub w okresie nieśności
Ptaki nieśne:
Szczepionka może być stosowana u kur niosek począwszy od 1 dnia życia.
3.8 Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Dostępne są dane dotyczące bezpieczeństwa i skuteczności, które wykazują, że szczepionka ta może być podawana tego samego dnia, ale nie może być mieszana z żywymi szczepionkami przeciw chorobie Newcastle. Brak informacji dotyczących bezpieczeństwa i skuteczności szczepionki stosowanej jednocześnie z innym weterynaryjnym produktem leczniczym, dlatego decyzja o zastosowaniu szczepionki przed lub po podaniu innego weterynaryjnego produktu leczniczego powinna być podejmowana indywidualnie.
3.9 Droga podania i dawkowanie
Podanie wziewne.
Szczepionka może być podawana drogą rozpylania, tzw. „gruba kropla” (coarse spray) lub jako aerozol.
Zalecany termin szczepień: od pierwszego dnia życia.
Przygotowanie szczepionki:
Tabletki szczepionki należy rozpuszczać wyłącznie w czystej wodzie (przegotowanej, zimnej). Nie używać wody ze śladowymi ilościami środków dezynfekujących lub detergentów.
W celu przygotowania szczepionki należy wyjąć tabletkę z blistra i wrzucić ją do wody. Należy odczekać 1-2 minuty do całkowitego rozpuszczenia się tabletki, a następnie delikatnie zamieszać, celem uzyskania jednorodności szczepionki.
Szczepić zwierzęta dopiero po całkowitym rozpuszczeniu tabletki.
Odtworzony produkt jest prawie klarowną, lekko mętną zawiesiną.
Szczepionki nie należy stosować, jeśli cała tabletka nie jest w pełni rozpuszczona lub nie rozpuszcza się w ogóle, ani jeśli tabletka ma niewłaściwy wygląd, taki jak zmiana koloru lub spuchnięta tabletka.
Nie należy używać tabletek z przebitych części blistra.
Nie należy zachowywać niewykorzystanej porcji szczepionki do użycia w innym dniu. Nie podawać zbyt małej dawki.
Po rekonstytucji szczepionkę należy zużyć w ciągu maksymalnie 2 godzin, a najlepiej natychmiast.
Zalecana objętość podczas rozpuszczania (w ml):
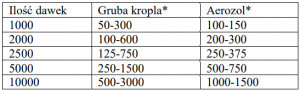
* dokładna ilość wody zależy od wydajności urządzenia rozpylającego.
Sprzęt:
Gruba kropla (coarse spray) – metoda ta pozwala szczepić kurczęta jednodniowe tuż po wylęgu w wylęgarni lub po wstawieniu do kurnika za pomocą zwykłego opryskiwacza ogrodniczego. Do szczepienia starszych ptaków należy użyć opryskiwacza elektrycznego lub zamgławiacza, które wytwarzają bardziej jednorodną kroplę. Średnica kropli nie powinna być mniejsza niż 100 µm.
Aerozol: metoda wymaga zastosowania opryskiwacza elektrycznego, wytwarzającego jednorodną kroplę o średnicy 40-100 µm. Stosowana jest do powtórnego szczepienia starszych ptaków.
Zalecenia dla prawidłowego podania:
Do mycia urządzeń rozpylających szczepionkę należy używać gotowanej, gorącej wody. Przed szczepieniem należy sprawdzić wydajność urządzenia rozpylającego.
Dysze rozpylające powinny znajdować się na wysokości 60-70 cm nad ptakami. Przed szczepieniem należy zredukować oświetlenie, wyłączyć wentylację i ogrzewanie.
W trakcie oraz po szczepieniu zapewnić ptakom spokój. Odpowiedź immunologiczna na antygen szczepionki zostanie zmniejszona w wyniku niewłaściwego przechowywania lub podawania.
3.10 Objawy przedawkowania (oraz sposób postępowania przy udzielaniu natychmiastowej pomocy i odtrutki, w stosownych przypadkach)
Badania potwierdziły bezpieczeństwo produktu nawet przy podaniu jednodniowym pisklętom SPF dawki 10-krotnie przewyższającej dawkę zalecaną (podanie do oka).
3.11 Szczególne ograniczenia dotyczące stosowania i specjalne warunki stosowania, w tym ograniczenia dotyczące stosowania przeciwdrobnoustrojowych i przeciwpasożytniczych weterynaryjnych produktów leczniczych w celu ograniczenia ryzyka rozwoju oporności
3.12 Okres (-y) karencji
Nie dotyczy
Zero dni.
4.1 Kod ATCvet:
QI01AA03
Szczepionka stymuluje czynną odporność przeciw zakaźnemu zapaleniu oskrzeli ptaków. Szczepionka
zawiera żywy, atenuowany szczep wirusa zakaźnego zapalenia oskrzeli ptaków, namnażany na
zarodkach kurzych SPF, oczyszczany przez wymrażanie, a następnie tabletkowany i pakowany w
blistry.
5.1 Główne niezgodności farmaceutyczne
Ponieważ nie wykonywano badań dotyczących zgodności, tego weterynaryjnego produktu leczniczego nie wolno mieszać z innymi weterynaryjnymi produktami leczniczymi.
5.2 Okres ważności
Okres ważności weterynaryjnego produktu leczniczego zapakowanego do sprzedaży: 2 lata.
Okres ważności po rekonstytucji zgodnie z instrukcją: 2 godziny
5.3 Specjalne środki ostrożności podczas przechowywania
Przechowywać w lodówce (2°C–8°C).
Chronić przed światłem.
5.4 Rodzaj i skład opakowania bezpośredniego
PTabletki (zawierające 1000, 2000, 2500, 5000 lub 10 000 dawek) pakowane są w dwuwarstwowe
blistry aluminiowe: warstwa Alum Soft Silver (PVC/PVDC) oraz warstwa Alum Silver (PVC).
Każdy blister zawiera 10 tabletek.
(PVC): polichlorek winylu; (PVDC): polichlorek winylidenu.
Pudełko tekturowe zawiera 1 blister (10 tabletek).
Niektóre wielkości opakowań mogą nie być dostępne w obrocie.
5.5 Specjalne środki ostrożności dotyczące usuwania niezużytych weterynaryjnych produktów leczniczych lub pochodzących z nich odpadów
Leków nie należy usuwać do kanalizacji ani wyrzucać do śmieci. Należy skorzystać z krajowego systemu odbioru odpadów w celu usunięcia niewykorzystanego
weterynaryjnego produktu leczniczego lub materiałów odpadowych pochodzących z jego zastosowania w sposób zgodny z obowiązującymi przepisami oraz krajowymi systemami odbioru
odpadów dotyczącymi danego weterynaryjnego produktu leczniczego.
PHIBRO ANIMAL HEALTH (POLAND) Sp. z o.o.
ul. Towarowa 28
00-839 Warszawa
Polska
14.07.2011 / 03.04.2017
ZAKAZ WYTWARZANIA, IMPORTU, POSIADANIA, SPRZEDAŻY, DOSTAWY I/LUB
STOSOWANIA, JEŻELI DOTYCZY
Nie dotyczy